来年度から機能性表示食品制度はどう変わるのか
10月18日に「第10回 機能性表示食品制度における機能性関与成分の取扱い等に関する検討会」が開催されました。
この日の検討会で、幾つかの重要な事項が概ね合意されたことで、今後の機能性表示食品制度の方向性が見えてきたので、その内容を追っていきます。
10回にわたる検討会から見えてきたこと
2016年1月に第一回の検討会が開催され、10回にわたって議論が行われてきたメインのテーマは二つです。
- 機能性関与成分における栄養成分の取り扱いについて
- 機能性関与成分が明確でない食品の取り扱いについて
この二つについて、10か月間にわたり検討を重ねてきて、ようやくその結果が出た、ということになります。
まず、栄養成分について今までの流れを確認してみます。
栄養成分としては、糖質・糖類、たんぱく質、脂質、ビタミン・ミネラルについて機能性表示食品に加えるか議論がされてきました。
中でも、ビタミン・ミネラルについては現時点では栄養機能食品制度のみで、汎用性が高くないことから、機能性表示食品に入るかどうかが注目されていました。
ビタミン・ミネラルは機能性表示食品の対象としない
検討会で議論された結果として、ビタミン・ミネラルは機能性表示食品の対象とはならないことで進めることとなりました。これは、この制度の方向性として大きなポイントです。
対象としない理由としては
- 過剰摂取の懸念がある
- 健康・栄養政策、他の制度との整合性などの兼ね合い
といったことが挙げられています。
さらに、「今後は、ビタミン・ミネラルについては栄養機能食品の制度において別途検討すべき」となっています。要するに、すでに栄養機能食品の制度があるのだから、機能性表示食品の対象とはしませんよ、と言うことです。
事業者団体からの提案も却下
ビタミン・ミネラルについては、何らかの表示ができないのか、と事業者団体から三つの提案がなされました。
一つ一つ見ていきましょう。
提案1:機能性表示食品に栄養機能の併記を認めていただきたい
- 既に栄養機能食品の制度があるので、機能性表示食品に栄養機能を表示したら、過剰摂取の原因になる恐れ
- 栄養機能食品制度があるので、消費者の誤認を招く
以上の理由により、却下
提案2:機能性表示食品で、成分の組み合わせによる3次機能の表示を認めていただきたい
- 複数成分の組み合わせは、単一の成分より専門的な判断が必要となる
- まずは単一の成分について整理することが先決
以上の理由により、却下
提案3:ビタミン・ミネラルの新しい機能について、栄養機能食品制度の枠組みの中で検討いただきたい
- 健康・栄養政策との整合性を図りつつ、栄養機能食品の制度で別途検討していくのが適当
以上のように、栄養機能食品の制度で検討する(ただし、その方法や時期については不明のまま)
これらの通り、ビタミン・ミネラルについては、機能性表示食品とは関係なく、今まで通り栄養機能食品制度の中で対応する方向性となりました。
ただし、どのように栄養機能食品制度を変えていくのか、といったところは議論されておらず、すぐに変更される様子はありません。
ガラパゴス化する機能性表示食品
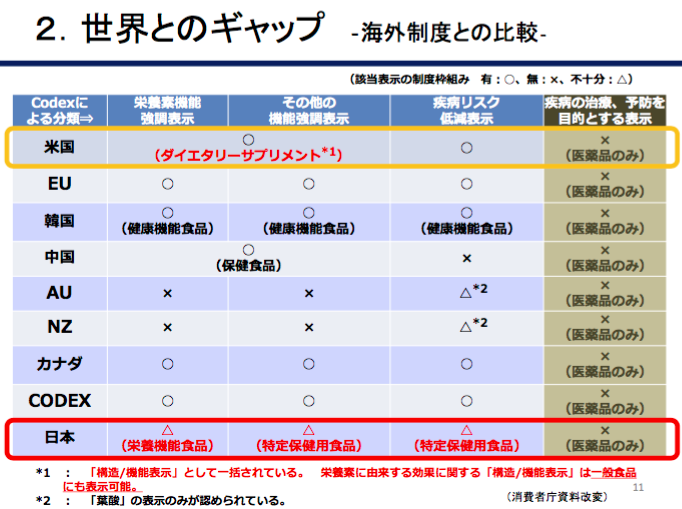
なお、海外ではどうなっているか、というと、ビタミン・ミネラルについて、多くの諸外国で栄養機能表示が認められています。
「内閣府:規制改革会議資料より抜粋」
アメリカのダイエタリーサプリメント、EUの健康強調表示などでは、ビタミン・ミネラルが成分として認められています。
例えばEUの場合
- ビタミンB12:「正常なエネルギー産生代謝の維持に寄与します」「ビタミンB12は、正常な心理機能に寄与します」
- 亜鉛:「正常な認知機能に寄与します」「正常な毛髪の維持に寄与します」
などといった文言が使用可能となっています。
検討会の結果、ビタミン・ミネラルを栄養機能食品の枠組みで対応する、となったことで、日本の制度がガラパゴス化していくようにも思えます。
現在の栄養機能食品は、国への届出も成分分析も必要なく、事業者の裁量で栄養機能を表示できる制度であり、諸外国と比べて十分な制度であるのか、といった疑問点も残ります。
機能性表示食品として適用できないのであれば、栄養機能食品制度の見直しもきちんと対応すべきではないか、と感じます。
機能性関与成分が明確でない食品はどうなるか
関与成分が明確でないものは、現行のガイドラインでは成分として認められていませんでしたが、新たにエキス(抽出物)が機能性表示食品の制度に加わることになります。
これには条件が付けられており
- 同等性を確保できる「指標成分」を複数設定すること
- 少なくとも1つの指標成分で作用機序が考察されていること
- 最終製品において、指標成分の分析方法の妥当性を検証する
- 崩壊性試験や溶出試験、重量偏差試験等を行い、製造過程の管理方法を届出資料に記載する
といった規定が新たに設けられることとなり、今まで以上に同等性の説明や品質管理が厳しくなる形となります。
詳細は11月25日に開催される11回検討会で報告書が出て、来年度のガイドラインに明記される予定です。
これまで以上にチェック体制も厳しくなる?
現在は、届出前に消費者庁が資料を確認し、指摘事項を出す形でチェックを行っていますが、今後は成分のチェックを含めた事後チェックについても重要になる、ぜひ加えて欲しいという委員からの要望も複数あがっていました。
さらには、広告の適正化や消費者教育を望む声も出ており、厳しく取り締まっていくべき、という声もあがっていました。
現時点でも消費者庁からの指摘が増えていますが、今後さらにチェックが厳しくなり、広告の取り締まりも厳しくなる、といった方向性を感じた検討会となりました。
制度開始から約2年間が経過し、一段落した機能性表示食品という制度は、また新たなステップに差し掛かっているのかも知れません。
次回の検討会の報告書では、具体的な方策などが盛り込まれる予定ですので、来年度以降の制度の動向については、追ってお話ししていきます。